Nanodropを使うと簡単に濃度が測れるけどどうなってるの?
NanodropはキュベットいらずでDNA濃度・タンパク質濃度を測れるので便利なのですが、何をどう測っているのかを理解しておくことは超重要です。
特に従来の分光計で使われるキュベットは1cmの光路長を持つのですが、Nanodropは明かに1cmの光路長を持っていないわけです。その辺の扱いはどうなっているのでしょうか?
Nanodropの特徴
- 光路長が0.2mmで、通常の分光光度計の10mmの1/50であるため、高濃度のサンプルも測定できます。
- 通常の分光光度計では、1cmの光路長があるため、試料濃度を薄める必要がありますが、Nanodropではその必要がありません。
Nanodropの使い方
- 「Sample type」ボックスで適切なタイプを選択します(例: BSAの濃度を測定する場合は、BSAを選択)。
- 両ペデスタルをペーパーティッシュで拭き取り、2µlのタンパク質試料を下部の台座に載せます。
- 「測定」を押します。通常、50mg/mlまでの濃度であれば希釈する必要はありません。
Nanodropの光路長は1mmですが、通常の10mm光路長の分光光度計で得られる吸収に変換されます。濃度と吸光度の相関にはBeer-Lambertの式が用いられます。
Nanodrop ND-1000の分光光度計は、1.0mmおよび0.2mmの光路長を使用し、標準的な分光光度計で測定できるサンプルの50倍以上の濃度を測定できます。
注意点:
- 各モジュールでのデータは、異なる光路長で正規化されています。
- タンパク質の吸収は、TryptophanとTyrosineから来ており、環境によって吸収特性が変わることがあります。
E1%とは、タンパク質の1%(10mg/ml)溶液を測定したときの吸光度です。これを使用して、未知のタンパク質の濃度を測定する際の係数を調べることができます。
Nanodropを使って正確な測定を行うためには、適切な係数を選択し、光路長を考慮すること
Nanodropの光路長は?
「Sample type」ボックスで「1Abs = 1mg/ml」を選択します。
BSAの濃度を測定する場合は、BSAを選択することができます)。また その他タンパク質(E & MW)」「その他タンパク質(E 1%) 」を選択して、タンパク質のモル消光係数、質量消光係数をそれぞれ入力し、吸光係数から濃度を自動計算することもできます。を選択すると、吸光度から濃度を自動計算することができます。
ペーパーティッシュで拭き取り、2µlのタンパク質試料を下部の台座に載せます。を載せます。測定」を押します。通常の分光光度計のように、タンパク質試料を希釈する必要はありません 通常の分光光度計のように試料を希釈する必要はありません。通常、50mg/mlまでの濃度であれば 50mg/mlまでは希釈する必要はありません。
サンプルの種類として「1Abs = 1mg/ml」を選択した場合、下のボックス「mg/ml」に280nmでのタンパク質の吸収が表示されます。Nanodropの光路長は1mmですが、通常の10mm光路長の分光光度計で得られる吸収に変換されることを覚えておいてください。(前述したように消衰係数を入力した場合は、直接濃度が表示されます)。
両ペデスタルを拭き、(特にタンパク質の場合、溶媒の蒸発とペデスタルへのタンパク質の付着を避けるため、測定が終わったらすぐに拭いた方がよい)次のバッファまたはサンプルを置く。同じバッファーで複数のサンプルを測定する場合、ブランキングは1回で済みますが、ペデスタルをきれいに保つために、間にブランキングを行うことをお勧めします。汚れた場合は、水をかけたり、濡れたティッシュペーパーで拭いてください。
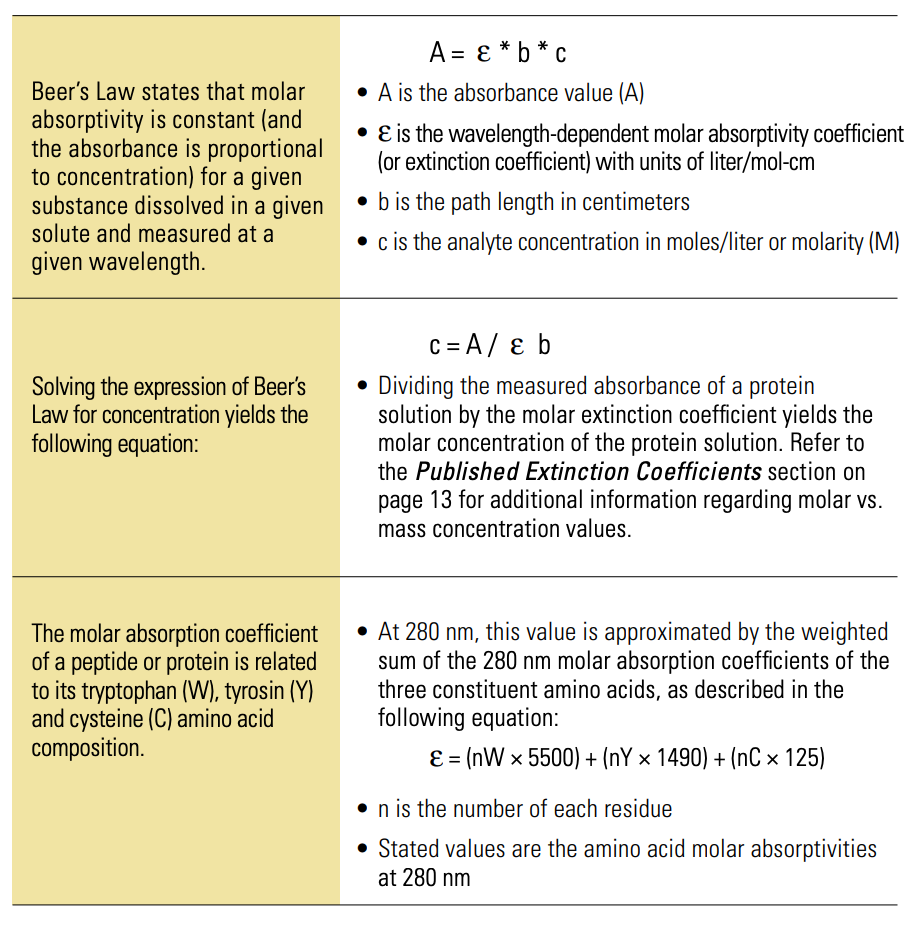
算出された吸光度を濃度と相関させるために、Beer-Lambertの式が用いられます。
A = E * b * c
ここで、Aは吸光度単位(A)、Eは波長依存のモル吸光係数(または消光係数)、単位はリットル/モル・cm、bは光路長(cm)、cは分析物濃度(モル/リットルまたはモル比(M))で表される。
NanoDrop® ND-1000 の分光光度計のために、1.0 mm および 0.2 mm の道は 10.0 mm の道を使用して標準的な分光光度計と比較されて使用されます。したがって、NanoDrop® ND-1000 分光光度計は、標準的な分光光度計で測定できるサンプルの50倍以上の濃度を測定することが可能です。
注)アーカイブファイルに記載されている吸光度データは、ソフトウェアの画面上に表示されたものを表しています。Nucleic Acid、Protein A280、Proteins and Labelsモジュールでは、データは1.0 cm (10.0 mm) パスで正規化されています。MicroArray、UV-Vis、Protein BCA、Protein Bradford、Protein LowryおよびCell Cultureモジュールでは、データは0.1 cm (1.0 mm)のパスで標準化されています。高吸光度のUV-Visサンプルでは、データは0.1 mmのパスで正規化されます。
Q
DNAの濃度を260nmで測定する場合、標準的な1cmの光路長ではなく、1mmの光路長でサンプルを測定しているため、ソフトウェアが自動的に補正を行います。OD 600 nmでの細胞培養の場合、ソフトウェアは同じことを行いません。代わりに、1mmの吸光度を表示します。なぜでしょうか?
A
この回答は、Nanodrop Technologies, Inc.のアプリケーションサイエンティストから電子メールでの回答として届いたものです。
「はい、Cell Culturesモジュールは現在10mmではなく1mmで表示されています。
注:アーカイブファイルに表示される吸光度データは、ソフトウェアの画面に表示されるように表現されています。Nucleic Acid、Protein A280、Proteins and Labelsモジュールでは、データは1.0 cm(10.0 mm)パスで正規化されています。MicroArray、UV-Vis、Protein BCA、Protein Bradford、Protein LowryおよびCell Cultureモジュールでは、データは0.1 cm (1.0 mm)のパスで標準化されています。高吸光度のUV-Visサンプルについては、データは0.1 mmのパスで正規化されます。
懸濁液中の微生物細胞培養について。
短い回答です。ND-1000は細菌増殖培養の推定に使用することができ、いかなる制限も他の分光光度計の制限と同様である。
長い答え 細菌培養の成長測定を取り巻く基本的な問題は、吸光分光光度計が懸濁液中の微粒子による光散乱を決定するよう求められていることです。この場合、透過率は古典的な意味での吸光度とは関係がありません。通常の真の吸光度条件下では、試料が実際に電磁エネルギーを吸収するため、分光光度計は互いに比較することができます。光散乱による透過率の減少の場合、測定値は特定の分光光度計の光学系と懸濁液中の細胞の種類に大きく依存します。細菌の増殖判定では、1cmの光路長のシステムでも、各システムの光学系のばらつきにより、大きく変動することがあります。ND-1000は、1mmの光路長を利用しているため、1cmのシステムよりも約10倍低い「吸光度」を表示します。しかし、先に述べたような理由から、その差は正確に10倍にはなりません。要は、ND-1000と「従来型」のスペックとの差は(光路長による10倍の差を除けば)、光路長1cmの分光光度計の差と同様であるということです。"
https://openwetware.org/wiki/Nanodrop
https://tools.thermofisher.com/content/sfs/brochures/Thermo-Scientific-NanoDrop-Products-Protein-Technical-Guide-EN.pdf
大変初歩の質問で申し訳ありません。
Nanodropでのタンパク質測定時のfactorの計算方法を具体的に教えて頂けませんでしょうか。
たとえば選択できるIgGではfactorが13.7になっていますがこれはどのようなリファレンスデータをもとにどのような計算式で求められますか?
Nanodrop関連の説明を検索したら、光路長の話だけでも「自動的に0.2mm光路長測定時の値を使って」とか「吸光度は10mm光路長換算で表示」とかNanodropの仕様の光路長が0.05~1mmとか、いろいろ出てきてよくわかりません。
当ラボの昔の人のノートでは係数14を使っている記録があるのですが、これはその溶液のIgGサブクラスの構成の違いとかそんな考え方ではおかしいでしょうか?
またよくでてくるE1%とはどういう意味でしょうか。
自分が今後関わる分野では、未知のタンパクを他の方法できちんと定量する方法ではなく、ある程度どこかで同等品のA280に対する濃度データを調べてNanodropのfactorに使う手順で濃度測定をするらしいのですが、こういう時の数値の一般的な調べ方ってありますか?
今後の各種factor計算の考え方の指標にしたいです。
曖昧で申し訳ありませんが答えられる範囲でお願いします。
こう言うのは実際実験に基づいて数値を決めることもあるかと思いますが、280nmの吸収はTryptophanとTyrosineの吸収からきているので、それに基づいて計算することが可能です。もちろん周りのアミノ酸のなどの環境で吸収特性が変わることがありますので、いくらかずれが生じることはあるとおもいます。
e1%は、そのタンパク質の1%(10 mg/ml)溶液を測定した時の吸光度、です。
実際は吸光度そのものではなくて、吸光度をもとに得られる係数ということですが、数字は同じで、係数として扱えるように単位が変わります。
Mass extinction coefficients (E1%)
The E1% is the absorbance at 280 nm of a 10 mg/mL solution in a 1-cm pathlength cuvette.



コメント